13 progrès à l'Institut de la Vision, 2e partie

Le voyage passionnant à travers les avancées majeures de la recherche fondamentale dans le domaine de la vision se poursuit dans cette deuxième partie dédiée à l'extraordinaire travail accompli à l'Institut de la Vision, au cours des treize dernières années. Alors que l'attente peut sembler interminable pour ceux qui endurent le fardeau des pathologies, l'espoir résiste grâce à cette institution française à l'aura internationale.
Mémo, article > 13 innovations majeures à l'Institut de la Vision, partie 1.
Rendre la vue avec la rétine artificielle
Lorsque les photorécepteurs ont disparu, est-il possible de les remplacer par un dispostif électronique ou prothèse rétinienne pour réintroduire des informations visuelles ? Les résultats des premiers essais cliniques ont été publiés fin 2019 avec la prothèse PRIMA, laissant place à de nombreux espoirs pour tous les patients concernés par des maladies dégénératives des photorécepteurs. En effet, ces essais viennent consacrer dix années de recherche et d'avancées, portées par Serge Picaud (Directeur de Recherche Inserm et Directeur de l’Institut de la Vision) et le Pr José-Alain Sahel à l'Institut de la Vision pour rendre la vue aux personnes devenues aveugles. La rétine artificielle, ou prothèse rétinienne, consiste à pallier la destruction des cellules photoréceptrices en réactivant électriquement les neurones qui envoient l'information au cerveau. Créée en 2011 par l’Institut de la Vision pour produire des prothèses sous-rétiniennes, l'entreprise Pixium Vision a ainsi développé PRIMA en partenariat avec le Pr Palanker de l’université de Stanford. Des tests positifs sur des primates non-humains réalisés par l’Institut de la Vision ont permis de lancer les premiers essais cliniques réalisés sur des personnes atteintes de DMLA. Les résultats ont dépassé les attentes puisque tous les patients ont retrouvé une capacité à relire des mots : une première en la matière ! Un essai international de phase III devrait permettre la commercialisation du dispositif.
En dix ans, l’Institut de la Vision réalise une partie du rêve de rendre la vue aux patients aveugles.
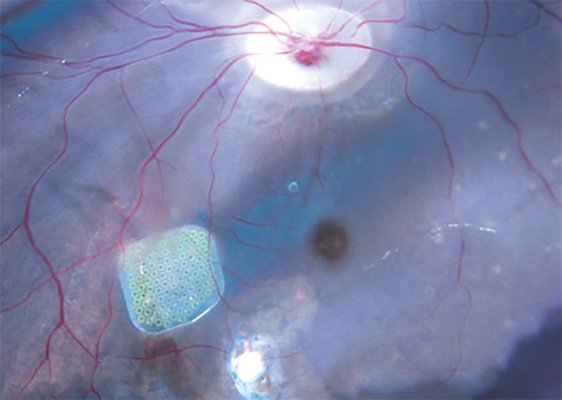
Prothèse sous-rétinienne Prima au fond d'œil © Institut de la Vision
Cécité, les espoirs de la thérapie optogénétique
La thérapie optogénétique repose sur l’expression de protéines photosensibles généralement issues d’algues pour restaurer une sensibilité à la lumière de la rétine des patients aveugles. Cette stratégie fut introduite à l’Institut de la Vision dans un partenariat de Serge Picaud et du Pr Sahel avec le Dr Botond Roska de l’Institut d’ophtalmologie de Bâle (Suisse). Le Pr Sahel fit venir le Dr Jens Duebel (Chercheur CNRS) de l’Institut de Bâle et Deniz Dalkara (Directrice de Recherche Inserm) depuis l’université de Berkeley, spécialiste des vecteurs de thérapie génique pour développer cette approche prometteuse pour rendre la vision aux personnes aveugles. Le principe de l'optogénétique consiste à modifier génétiquement par thérapie génique les cellules résiduelles de la rétine afin de les rendre à nouveau sensibles par la lumière par la protéine d’algues. Après des essais concluants sur des tissus humains, des rongeurs et des primates non-humains, les premiers essais cliniques ont commencé avec des patients atteints de rétinopathie pigmentaire à l’hôpital de la vision des Quinze-Vingts sous la direction de la Pr Isabelle Audo, du Dr Elise Boulanger-Scemama et en partenariat avec l’entreprise, Gensight Biologics. La sensibilité de cette protéine étant plus faible que celle de nos photorécepteurs naturels, les chercheurs ont dû développer un dispositif intelligent de capture d’image combiné à une stimulation à forte luminance. Les patients doivent ainsi porter ces lunettes dotées de caméra pour augmenter l'intensité lumineuse des images. Certains patients aveugles atteints de rétinopathie pigmentaire ont ainsi retrouvé partiellement la vue grâce à la protéine d’algues. La poursuite de l’évaluation fonctionnelle des patients permettra de définir l'acuité visuelle procurée par cette nouvelle forme de thérapie.

Visualisation au microscope d'une fovéa, la partie centrale de la rétine. La fovéa est la région de l'œil responsable de l'acuité visuelle, nous permettant de lire, conduire ou encore reconnaître des visages. © Institut de la Vision
Œil et rétinopathie, du côté de la thérapie cellulaire
Produire des cellules rétiniennes à partir de cellules souches pluripotentes humaines et les greffer dans l’œil pour remplacer les cellules défectueuses : tel est l'objectif de l’équipe d’ Olivier Goureau (Directeur de Recherche INSERM). Forte de ses connaissances sur le développement de la rétine, cette équipe de chercheurs a réussi en partenariat avec l’équipe de la Dr Christelle Monville de I-Stem à créer puis à transplanter un “patch” de cellules de l'épithélium rétinien dérivées de cellules pluripotentes humaines. Cette thérapie génique a dans un premier temps été évaluée sur une lignée de rats porteuse d’une mutation exprimée dans cet épithélium rétinien et causant la perte des photorécepteurs comme il peut être également observé chez certains patients atteints de rétinopathie pigmentaire avec des mutations similaires. Le résultat étant positif sur la survie des photorécepteurs, la non toxicité du patch de cellules a ensuite été évaluée chez des primates non-humains dont le système immunitaire est proche de celui de l’homme. Depuis, un essai clinique de thérapie cellulaire est en cours sur des patients atteints de rétinopathie pigmentaire dont les mutations causales sont exprimées sélectivement dans l’épithélium pigmentaire. Pour cette première clinique, les résultats préliminaires sont très encourageants et les résultats complets devraient prochainement être publiés. Cette thérapie cellulaire testée dans un premier temps sur des patients atteints de rétinopathie pigmentaire pourrait voir son champ d’application s’élargir car certaines pathologies comme la DMLA sont parfois attribuées à un dysfonctionnement des cellules de l’épithélium rétinien.
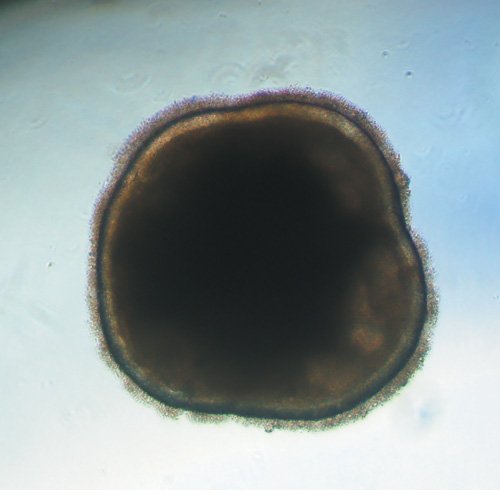
Organoïde de rétine obtenu à partir de cellules souches humaines © Institut de la Vision
L'imagerie rétinienne haute résolution
Saviez-vous qu'une infime partie (quelques photons) de la lumière que nous recevons se réfléchit et ressort de l’œil ? Aujourd’hui, l’enjeu consiste à extraire les informations de cette lumière grâce à un ensemble de technologies. Aux côtés de l’optique adaptative ont été développées des techniques originales comme la tomographie de cohérence optique plein champ, l’illumination structurée et l’holographie Doppler, offrant de nouvelles vues sur la rétine. Résultat : grâce au travail du Pr Paques, du Dr Kate Grieve (Directrice de Recherche Inserm) et de leurs équipes, il est désormais possible de visualiser de façon non invasive les différentes couches cellulaires de la rétine et de la cornée sur de grands champs. La résolution obtenue permet d’observer très précisément les altérations des cellules en cause dans les maladies de la rétine (photorécepteurs, épithélium rétinien, macrophages…). Ces nouvelles technologies offrent la possibilité d'élucider de nouveaux phénomènes dans des pathologies comme la DMLA ou les maladies rares. Leur précision permettant de suivre l’évolution des maladies sur des temps courts, il devient ainsi possible de faire des essais cliniques même sur ces pathologies réputées d’évolution lente. Grâce à ces nouvelles technologies, l’accès optique à la rétine et à ses vaisseaux font également de la rétine un tissu modèle pour visualiser des symptômes précoces de maladies comme l’hypertension artérielle mais aussi peut-être des maladies neurodégénératives qui affectent aussi la rétine comme la maladie d’Alzheimer.
Lire l'article "Dr Kate Grieve, Optoretina et l'imagerie rétinienne haute résolution" >
La sonogénétique, déclencher la vue grâce aux ultrasons
Si les approches ci-dessus visent à restaurer la vision des patients ayant perdu leurs photorécepteurs, rien ne permet actuellement de compenser la perte de vision des patients perdant le nerf optique ou lien œil-cerveau. Les chercheurs ont posé la question suivante : serait-il possible de redonner à ces aveugles « la vue » en activant par ultrasons directement les neurones de la partie de leur cerveau responsable de la vision ? Aussi incroyable qu’elle paraisse, cette question n’est pourtant plus du domaine de la science-fiction grâce aux travaux de Serge Picaud à l’Institut de la Vision. Avec son collègue Mickaël Tanter, du laboratoire Physique pour la médecine (ESPCI Paris/PSL Université/Inserm/CNRS), spécialiste des ultrasons, ils sont à l’origine du projet Soundvision. Leur stratégie a consisté à modifier les neurones du cortex pour les rendre sensibles aux ultrasons, en leur faisant exprimer par thérapie génique une protéine mécanosensible. En réponse à la pression acoustique exercée par les ultrasons, cette protéine permet d’activer les neurones du cortex visuel sur des rongeurs. Les chercheurs ont montré en utilisant un apprentissage associatif du type reflexe de Pavlov que la souris perçoit de la lumière à la stimulation ultrasonore de son cortex visuel. En effet, elle a appris à associer un flash lumineux avec un apport d’eau, et elle léchera de la même manière le tube d’eau qu’il s’agisse d’un flash lumineux ou une stimulation ultrasonore du cortex visuel. Bien sûr, l’animal a ce comportement seulement si le cortex visuel a reçu la thérapie génique pour faire exprimer la protéine mécanosensible. Si la route sera longue avant une implémentation chez l’homme, les espoirs portés par la sonogénétique sont immenses.

© Alexandre Dizeux/Physics for Medicine Pari
Analyses et tests visuels : Streetlab, l'orientation spatiale au bénéfice thérapeutique
Pour l’évaluation des stratégies thérapeutiques, il devient de plus en plus important d’évaluer le bénéfice thérapeutique pour le patient avant d’obtenir la décision des agences sur l’acceptation des traitements. C’est pourquoi le Pr Sahel a voulu créer la plateforme d’évaluation Streetlab. Véritable studio de cinéma avec un décor escamotable de rue, Streetlab permet de monitorer les déplacements d’un patient dans l’espace tout en contrôlant la position de son regard pour reconstituer son champ de vision et être capable de générer son avatar. Cette structure unique est maintenant impliquée dans de nombreux essais cliniques dont ceux sur la restauration visuelle par optogénétique ou prothèse rétinienne. Cette plateforme a ainsi pu démontrer le bénéfice du traitement de thérapie génique, Luxturna, développé par l’entreprise américaine Spark. En faible luminance, les patients sont incapables de se déplacer dans un labyrinthe alors qu’ils le parcourent en toute facilité et autonomie quelques mois après le traitement. L’équipe a mainetenant développé et validé un système d’évaluation utilisant la réalité virtuelle, qui suscite une fort intérêt de nombreuses équipes internationales.Sur cette plateforme Streetlab, le Dr Angelo Arleo (Directeur de Recherche CNRS) a également démontré que les patients âgés se repéraient dans l’espace non plus sur des indices locaux mais sur des indices géométriques globaux de la pièce, potentiellement plus simples à extraire visuellement et à mémoriser. Ils ont aussi tendance à tenir compte des informations en position basse sans que cela soit lié à une question de posture. La définition de ces phénomènes devrait aider au développement de solutions visant à améliorer l’autonomie et la qualité de vie des personnes âgées dans notre société.
Un traitement du glaucome mieux toléré
Le Pr Christophe Baudouin (PU-PH Université de Versailles Saint-Quentin-en-Yvelines Hôpital de la vision des Quinze-Vingts.) a travaillé sur la tolérance des traitements par gouttes pour le glaucome. La majorité des glaucomes résultent d’une augmentation de la pression intraoculaire ce qui affecte la viabilité des cellules ganglionnaires connectées au cerveau. Le glaucome est la seconde cause de cécité dans le monde après la cataracte car cette augmentation de pression intraoculaire intervenant avec l’âge est très insidieuse car non douloureuse. Des traitements très efficaces permettent de réduire cette pression intraoculaire et d’éviter la perte neuronale consécutive. Cependant, l’observance à long terme était un problème d’autant que l’application des gouttes pendant des dizaines d’années entraînaient une inflammation de la surface oculaire avec des douleurs oculaires persistantes pour plus de la moitié des patients. Le Pr Baudoin s’est alors intéressé avec son équipe à cette question de la tolérance des gouttes pour le glaucome. Ils ont montré qu’un conservateur est à l’origine d’une toxicité cellulaire et de l’inflammation oculaire consécutive. Cette découverte a permis, en collaboration avec l'industrie pharmaceutique notamment l’entreprise française Théa, de développer de nouveaux collyres, sans conservateur, pour mieux traiter les patients atteints de pathologies comme le glaucome et leur éviter l’apparition de douleurs oculaires chroniques.
Rédaction Serge Picaud & Pr José-Alain Sahel - Institut de la Vision
Soutenez la recherche, soutenez l'Institut de la Vision >

À lire aussi
Douleur oculaire, une prise en charge unique au CHNO des Quinze-Vingts
La sécheresse oculaire est l’un des premiers motifs de consultation dans les cabinets d’ophtalmologie&nbs

L'Institut de la Vision, histoire d’une pugnacité collective
1ere partie de l'histoire de l'Institut de la Vision - Paris.

Phénotypage, génotypage, intelligence artificielle, jumeaux numériques... une nouvelle ère pour la médecine personnalisée
Véritable enjeu de santé publique, les pathologies rétiniennes sont à l’origine de divers handicaps visuels, et de répercussions variables sur la vie sociale et professionnelle des patients concernés.

13 avancées majeures à l'Institut de la Vision
Si le temps de la recherche paraît souvent très long, et tout particulièrement pour les patients atteints de pathologies ne disposant d'aucun traitement, la recherche sur les maladies de la vision a








