Douleur oculaire, mieux comprendre ses mécanismes pour mieux la traiter à l'Institut de la Vision

PARTIE 1
Tel un signal d'alarme, la douleur oculaire est particulièrement utile pour protéger l'œil des agressions et préserver les tissus. Or, lorsqu'elle s'installe durablement et devient chronique, la douleur s'avère particulièrement difficile à traiter, avec de fortes répercussions sur la qualité de vie des patients. À l’Institut de la Vision, l’équipe du Pr Christophe Baudouin est une des rares au monde, en tout cas la seule en France, à s’intéresser à la douleur oculaire et lui consacrer un axe de recherche. Car mieux connaître et comprendre les mécanismes cellulaires et moléculaires impliqués dans l’initiation et la chronicisation des douleurs oculaires permettra d'aider au développement de nouvelles thérapeutiques visant à stopper ces douleurs. Le Gui de la Vue fait le point avec le Dr Annabelle Réaux-Le Goazigo, neurobiologiste et chercheuse Inserm, membre de cette équipe à l'Institut de la Vision.
À l’Institut de la Vision, les récents travaux de l’équipe du Pr Christophe Baudouin et du Dr Stéphane Mélik Parsadaniantz ont d'ores et déjà permis de faire un bond certain dans la compréhension des douleurs oculaires, leur mode de propagation et leur chronicisation. Ceux du Dr Annabelle Réaux-Le Goazigo par exemple, chercheuse Inserm dans cette équipe à l’Institut de la Vision, ont permis dans un premier temps de mieux identifier et caractériser les neurones en cause dans ces pathologies, en déterminant leur distribution en 3D dans le ganglion trigéminal (ganglion de Gasser chez l’homme). Par le biais d'images haute résolution, ces travaux ont également permis de quantifier très précisément la population des neurones cornéens qui ne représente que 5% de la population totale des neurones du ganglion trigéminé. “La cornée est le tissu le plus densément innervé du corps humain. Cette innervation cornéenne est assurée par des neurones qui sont localisés dans une structure appelée le ganglion trigéminal. Et ces neurones ont la particularité d’être des neurones sensoriels appelés neurones en T ayant une terminaison périphérique (au niveau de la cornée) et une terminaison centrale (qui se projettent dans le tronc cérébral), faisant ainsi le lien entre la périphérie (cornée) et le cerveau. Ainsi, l'activation des terminaisons cornéennes conduit à une activation des neurones du tronc cérébral et cette information nociceptive est ensuite transmise dans d’autres centres nerveux pour être intégrée dans le cortex somatosensoriel”, explique le Dr Réaux-Le Goazigo. Ainsi lorsque de façon récurrente la cornée va subir des altérations ou des abrasions, en particulier chez les patients souffrant du syndrome de l'œil sec - une pathologie qui touche dans le monde presque 30% de la population des plus de 50 ans -, les terminaisons nerveuses vont être sollicitées en continu, entraînant une douleur chronique.
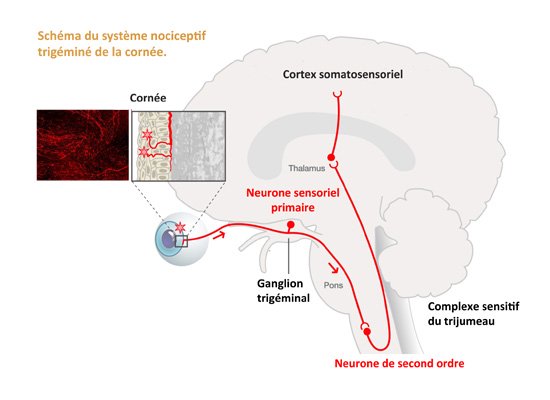
Schéma du système nociceptif trigéminé de la cornée
L'enregistrement de l'activité des nerfs cornéens
La douleur oculaire peut alors être de type inflammatoire par excès de nociception, c'est-à-dire qu'à la suite d'une lésion du tissu cornéen, une réaction inflammatoire se développe, sollicitant les cellules immunitaires dont l'activité va stimuler les nerfs et ainsi activer la voie nociceptive. La douleur oculaire peut également être de type neuropathique, c'est-à-dire que ce sont les nerfs eux-mêmes qui présentent une altération fonctionnelle. “Pour caractériser plus précisément la nature de la douleur oculaire, nous avons aujourd'hui recours à des outils très performants permettant de réaliser une imagerie de l’innervation et de l’inflammation cornéenne chez le patient”explique la neurobiologiste. Est pour cela utilisée la microscopie confocale in vivo (IVCM), un microscope bien particulier qui, appliqué sur l’œil du patient, permet de visualiser s'il existe des altérations de l’innervation cornéenne associées ou non à des symptômes douloureux. “Ce microscope confocal in vivo est également utilisé dans l’évaluation de nos modèles animaux. Nous sommes tout à fait capables de quantifier les altérations morphologiques des nerfs cornéens et de quantifier l'inflammation cornéenne. L’imagerie de la surface oculaire par IVCM est très précieuse car si des traitements topiques antalgiques sont disponibles pour l’homme, nous pourrons évaluer leur capacité à restaurer les anomalies morphologiques des nerfs cornéens”, ajoute le Dr Réaux-Le Goazigo. Et de préciser : “Nous avons récemment développé des outils permettant de réaliser l’enregistrement de l'activité électrique des nerfs cornéens dans nos divers modèles précliniques de sécheresse et de douleur oculaire. Cette approche nous a permis de montrer qu’une douleur oculaire chronique s’accompagne d’une augmentation de l'activité électrique des nerfs cornéens”.
Les altérations cellulaires et moléculaires dans le ganglion trigéminal en lien avec une douleur oculaire
L'équipe de l'Institut de la Vision est ainsi la seule équipe au monde à réaliser ces enregistrements de l'activité électrique des nerfs cornéens chez la souris. Et ces données sont précieuses pour les chercheurs car elles permettent de caractériser précisément l'activité de ces nerfs cornéens, qui sera différente en fonction du statut douloureux (douleur aiguë ou douleur chronique). “Si l'on reprend nos connaissances actuelles de la douleur en général, l'hypothèse est de se dire que ces neurones nociceptifs cornéens, alors hyperactivés, vont se mettre à exprimer des molécules différentes, comparés à un animal naïf, sans nociception oculaire. Nos travaux de recherche fondamentale ont ainsi permis de mettre en évidence des altérations cellulaires et moléculaires dans ce ganglion trigéminé en montrant entre autres une augmentation de l’expression de marqueurs pro-inflammatoires et de marqueurs de souffrance neuronale dans cette structure”, témoigne le Dr Réaux-Le Goazigo. Ainsi, une douleur oculaire a non seulement un impact en tant que tel sur la cornée, facilement visualisable chez l'homme et l'animal, mais également dans ce ganglion trijumeau. “Parce que nous sommes capables de mesurer l'expression de certains marqueurs inflammatoires ou impliqués dans la transmission de l’information nociceptive dans ce ganglion, nous avons ensuite ciblé ces molécules d’intérêt sur nos modèles précliniques par des instillations topiques : nous avons constaté que ces traitements pharmacologiques diminuaient non seulement les marqueurs inflammatoires, mais également l’hypersensibilité cornéenne”.

© Institut de la Vision - SU/LArdhuin
La douleur, de la cornée jusqu'au tronc cérébral
À l'Institut de la Vision, les chercheurs ont ainsi réussi à mieux comprendre les voies nociceptives mises en jeu dans la douleur oculaire et plus précisément les changements moléculaires qui s’opéraient non seulement dans la cornée mais également dans le ganglion trigéminal. Mais ils sont allés plus loin encore, car les changements qui s'opèrent dans les neurones ne se limitent pas au ganglion trigéminal. Les chercheurs ont démontré qu’une douleur oculaire chronique impactait des structures du système nerveux central, et en particulier le complexe sensitif du trijumeau qui se trouve dans le tronc cérébral. “Dans nos modèles précliniques de nociception cornéenne, nous avons pu mettre en évidence une plasticité dans le complexe sensitif du trijumeau, qui se manifeste par une activation neuronale et une réorganisation spatiale des cellules microgliales (des cellules immunitaires que l'on retrouve dans le système nerveux central). Nous savons aujourd'hui très bien que lorsqu'une douleur aiguë devient chronique, ces mécanismes centraux y participent pleinement”,explique la chercheuse Inserm. Les récentes découvertes de l'équipe montrent très clairement que dans un contexte de douleur chronique se met en place une activation ou un dérèglement du fonctionnement de ces cellules dans les régions cérébrales impliquées dans les voies de la douleur. Ces mécanismes cellulaires pourraient être responsables de la persistance de la douleur oculaire. “La question maintenant, après avoir identifié les mécanismes neuro-inflammatoires qui se produisaient au niveau de la cornée, du ganglion trigéminé et du cerveau, est de trouver comment les bloquer. Si l'on arrive à les bloquer de façon préventive ou réduire cette activation neuronale et cette inflammation, nous serons alors probablement capables d’éviter l’apparition ou la chronicisation d’une douleur oculaire”, ajoute le Dr Réaux-Le Goazigo.
Lisez la suite PARTIE 2 la semaine prochaine !

En photo : Dr Annabelle Réaux-Le Goazigo, du centre de recherche de l'Institut de la Vision, INSERM / CNRS / Sorbonne Université. © Institut de la Vision - SU/LArdhuin
Photo en tête d'article © Institut de la Vision - SU/LArdhuin
À lire aussi
Douleur oculaire, une prise en charge unique au CHNO des Quinze-Vingts
La sécheresse oculaire est l’un des premiers motifs de consultation dans les cabinets d’ophtalmologie&nbs

Le Guide de la Vue, édition mars 2022
Le Guide de la Vue Le mag N°33 vient de sortir !

Les douleurs oculaires, thème majeur de la nouvelle WebTV de l’Institut de la Vision
Parce qu'elles comptent parmi les principaux motifs de consultation chez l'ophtalmologiste, les douleurs oculaires étaient le sujet de la 6e WebTV de l'Institut de la Visi








