13 avancées majeures à l'Institut de la Vision

Si le temps de la recherche paraît souvent très long, et tout particulièrement pour les patients atteints de pathologies ne disposant d'aucun traitement, la recherche sur les maladies de la vision avance pourtant à vive allure à l’Institut de la Vision. Voici les treize dernières années racontées au travers d’une sélection de treize progrès majeurs en matière de lutte contre la cécité et les maladies de la vision, histoire d'en prendre toute la mesure... Dans cette première partie, nous mettrons en lumière six de ces progrès majeurs qui ont eu lieu à l'Institut de la Vision.
Transparisation des tissus et binocularité
La vision repose sur l’extraction des informations visuelles importantes dans les images au niveau de la rétine pour les envoyer sous forme compressées via le nerf optique au cerveau qui devra ensuite reconstituer les images perçues. Jusqu'à présent, suivre les diverses projections des neurones rétiniens sur le cerveau était très complexe et laborieux. l'Institut de la Vision a contribué au développement de nouvelles technologies d’imagerie pour observer l’ensemble de ces projections sur le cerveau entier toujours connecté aux yeux. L’Institut fut ainsi le premier centre au monde à utiliser un microscope dit « à feuillet de lumière ». Après avoir rendu les tissus fixés transparents par une stratégie chimique, l’équipe du Dr Alain Chédotal (Directeur de Recherche Inserm) a pu utiliser cette technologie pour visualiser les tissus dans des embryons entiers pour suivre le développement embryonnaire humain avec un intérêt spécifique pour l’œil humain. Avec le Dr Fillipo Del Bene (Directeur de Recherche Inserm), ils ont également étudié l’apparition de la binocularité dans la chaine de l’évolution, à savoir quand les champs visuels des deux yeux se superposent et vont se projeter dans le même hémisphère du cerveau. Si classiquement, il était convenu que cette binocularité était apparue après la sortie de l’eau du règne animal, ces deux chercheurs ont trouvé certains poissons présentant cette signature d’une binocularité en rupture complète avec le dogme très ancien. La technique de transparisation des tissus a été adaptée par l’équipe du Pr Michel Paques (PU-PH Sorbonne Université-Hôpital de la vision des Quinze-Vingts.) qui peut maintenant perméabiliser des yeux entiers humains de patients adultes. La prouesse tient à la transparisation de tous les tissus de l’œil même la sclère et l’épithélium rétinien remplis de pigments de mélanine. La technique peut maintenant s’appliquer à des yeux de patients atteints de différentes pathologies sans rompre l’anatomie de l’œil.
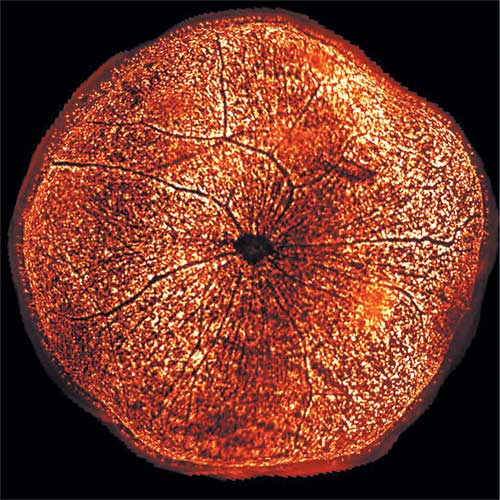
Image 3D d'un œil de souris transpiré. Les cellules ganglionnaires sont les petits points orange tapissant la surface de la rétine. Le disque noir au milieu est l'entrée du nerf optique. © Institut de la Vision
Les circuits de la vision mis en lumière
La vision est un système particulièrement complexe qui est encore loin d'avoir délivré l'intégralité de ses mystères. Si l'on connaît aujourd'hui la composition des circuits neuronaux de la rétine et du cerveau dans le processus de vision, il est essentiel d'en comprendre le développement et le fonctionnement afin de mieux appréhender et, surtout, mieux traiter les pathologies visuelles associées. C'est ainsi qu'ont été mises en place à l'Institut de la Vision, avec Jean Livet (Directeur de Recherche Inserm), de nouvelles méthodologies d'ingénierie génétique et d'imagerie pour suivre l’émergence des cellules du système visuel. En 2014, un système de marquage multicolore inédit a permis d'identifier et caractériser efficacement les neurones issus de chaque cellule souche neurale. Les équipes ont ensuite réussi à mettre au point une approche de microscopie permettant de visualiser ce lignage cellulaire et cette technologie de traçage cellulaire dans le tissu nerveux, jusqu'alors inaccessible, et ce avec une précision sans précédent.
En parallèle, Olivier Marre (Directeur de Recherche Inserm) a questionné le fonctionnement des cellules de la rétine. Il a ainsi montré que certaines cellules ganglionnaires qui extraient l’information visuelle pour la transférer au cerveau, peuvent posséder plusieurs fonctions suivant leur position par rapport à un objet : 1) définir sa position, 2) mesurer sa vitesse de déplacement pour les cellules plus éloignées de sa position. Ensuite, présentant de véritables images naturelles à la rétine isolée (paysage, immeuble…), il a montré que certaines de ces cellules ganglionnaires répondaient à la présence d’un contraste dans leur champ visuel comme le bord d’un immeuble. Ces avancées permettent de mieux comprendre le développement rétinien et cérébral ainsi que de définir comment la rétine compresse les informations visuelles à envoyer au cerveau.
Vers une meilleure compréhension de la DMLA
Véritable enjeu de santé publique, la dégénérescence maculaire liée à l’âge, DMLA, est aujourd'hui la première cause de malvoyance après 50 ans dans les pays développés : elle affecte environ 8% de la population, dont 25 à 30% des personnes âgées de plus de 75 ans, et consiste en une perte progressive de la vision centrale. Outre les facteurs de risque, lumière et tabagisme, la DMLA présente également un risque génétique lié à l’expression de certains facteurs de prédisposition génétique. Ces facteurs de prédisposition génétique codent pour des protéines impliquées dans les processus inflammatoires en cohérence avec l’observation dès 2007 dans la rétine malade (DMLA forme sèche ou humide) d’une accumulation anormale sous la rétine de macrophages, ces cellules inflammatoires dont le rôle est normalement d'éliminer les bactéries. Depuis 2012, à l'Institut de la Vision, l’équipe de Florian Sennlaub (Directeur de Recherche Inserm) a élucidé les mécanismes moléculaires liant les facteurs de prédisposition génétique à l’accumulation de ces macrophages devenant toxiques pour les photorécepteurs. Ces découvertes constituent une avancée majeure dans la compréhension de la maladie car elles permettent d’envisager le développement de nouvelles stratégies thérapeutiques pour la DMLA voire pour d’autres pathologies des photorécepteurs.

Une thérapie contre la rétinopathie pigmentaire
On estime aujourd'hui à 30 000 le nombre de personnes touchées en France par la rétinopathie pigmentaire, avec une prévalence d'environ 1/4000 naissances. Elle est l'une des formes les plus courantes de maladies génétiques dégénératives de la rétine. Elle se caractérise notamment par la perte progressive des photorécepteurs (cônes et bâtonnets) et un dysfonctionnement de l'épithélium pigmentaire. Pour rappel, les cônes sont en charge de la vision des couleurs, tandis que les bâtonnets sont responsables de la vision nocturne. Si la rétinopathie pigmentaire est caractérisée dans un premier temps par une perte des bâtonnets, la dégénérescence des cônes suit dans un second temps bien que ces derniers ne soient pas initialement touchés par l'anomalie génétique. La conséquence pour le patient est une dégradation progressive périphérique puis centrale de la vision jusqu'à la cécité totale. Le Pr Sahel (PU-PH Sorbonne Université-Hôpital de la vision des Quinze-Vingts, Directeur de l’Institut de la Vision jusqu’en 2020) avait démontré l’existence d’un facteur de survie expliquant le phénomène. Il fit alors venir le Dr Thierry Léveillard (Directeur de Recherche Inserm) et leur équipe découvrira ce facteur de survie des cônes : RdCVF (pour Rod-derived Cone Viability Factor). Ce facteur fabriqué principalement par les bâtonnets maintient la survie des cônes, sa disparition à la disparition des bâtonnets explique la destruction secondaire des cônes. Pour empêcher cette perte secondaire des cônes, Thierry Léveillard (Directeur de Recherche Inserm) et José-Alain Sahel ont alors établi qu'un traitement par thérapie génique pour réintroduire le facteur RdCVF permet, chez l'animal, de ralentir l'évolution de la maladie, l’extrapolation à l’homme suggérant que les patients pourraient garder une vision de qualité toute leur vie. Le Pr Sahel resté très impliqué dans ce travail a créé avec le Dr Léveillard la société SparingVision pour traduire ces résultats en clinique. Un premier essai clinique de phase I/II a commencé en 2023. Mené à l’hôpital des Quinze-Vingts et aux Etats-Unis, pour des patients atteints de rétinopathie pigmentaire à un stade très avancé, cet essai coordonné par la Pr Isabelle Audo (PU-PH Sorbonne Université-Hôpital de la vision des Quinze-Vingts) a déjà montré l’absence de toxicité de la plus faible dose du vecteur viral. Ce traitement pourrait devenir un traitement indépendant du gène muté pour les patients atteints de rétinopathie pigmentaire.
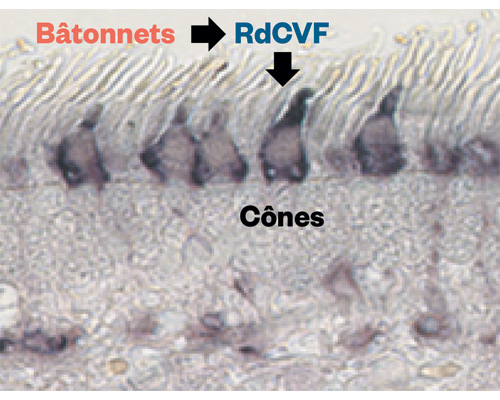
RdCVF : Rod-derived cone viabilty factor © Institut de la Vision.
Le point sur la neuropathie optique héréditaire de Leber (Nohl)
La neuropathie optique héréditaire de Leber résulte de mutations génétiques sur l’ADN mitochondrial. Etonnamment, bien que les mitochondries soient présentes dans toutes les cellules du corps humain, cette pathologie se caractérise uniquement par une baisse brutale de la vue jusqu'à la perte de la vision, sur les deux yeux. La perte de vision résulte d’une dégénérescence des cellules ganglionnaires qui envoient les informations visuelles au cerveau et forment le nerf optique. La maladie affecte principalement les hommes dans 80% des cas et se manifeste surtout entre 15 et 30 ans. S'il n'existe pour le moment aucun traitement permettant de prévenir ou stopper la baisse d'acuité, de nombreux espoirs sont portés par la thérapie génique afin de corriger par injection intravitréenne l'anomalie au sein des mitochondries. Convaincue par le Pr Sahel de rejoindre l’Institut de la Vision, la spécialiste des mitochondries, Marisol Corral-Debrinski (Directrice de Recherche CNRS) a développé sur l’animal cette thérapie génique particulière pour que le traitement puisse cibler les mitochondries. L’entreprise Gensight Biologics, issue de l’Institut de la Vision, a développé le vecteur thérapeutique de grade clinique, le GS010. Plusieurs études cliniques ont démontré l’efficacité du traitement avec une amélioration moyenne d'acuité supérieure à 15 lettres dans l’œil injecté ainsi qu'une amélioration de la qualité de vie des patients. L’amélioration se propageant dans l’œil non injecté initialement considéré comme le contrôle, les agences réglementaires ont demandé une nouvelle étude clinique dans laquelle certains patients ne seraient pas injectés avec le vecteur pour constituer un véritable groupe de patients contrôle placebo. Ce traitement ouvrirait la voie au traitement de la neuropathie optique de Leber mais potentiellement au traitement d’autres maladies mitochondriales.
Mieux soigner la douleur oculaire
La sécheresse oculaire est l'un des premiers motifs de consultation chez l’ophtalmologiste : caractérisée par une douleur à intensité variable, cette pathologie concerne entre 5 et 35% des personnes de 50 ans et plus. Elle compte parmi les douleurs oculaires fréquentes, dont les causes sont multifactorielles (climatisation, pollution, allergies, travail sur écran, etc.) et les traitements, peu nombreux, à l'efficacité limitée. C'est pourquoi la création d’une équipe par le Pr Chistophe Baudouin et sa direction actuelle à l'Institut de la Vision, par la Dr Annabelle Reaux-le-Guazigo (Chercheur Inserm) est particulièrement importante pour mieux comprendre les mécanismes de ces douleurs oculaires. L’équipe a en particulier découvert le rôle de l'inflammation chronique dans le dessèchement oculaire. En partenariat avec des industriels, elle a aussi pu démontrer sur des modèles animaux l’efficacité de collyres contenant des bloqueurs des enképhalinases. Dans une continuité translationnelle avec le service du Pr Baudouin, il a pu être montré que les nerfs cornéens présentent les mêmes modifications chez les patients et les modèles animaux. La création d'un centre de prise en charge de la douleur oculaire par le Pr Baudouin au sein de l'hôpital des Quinze-Vingts et l'étude de nouveaux biomarqueurs sont autant d'espoirs d’améliorer la douleur des patients atteints de ces maladies oculaires chroniques.
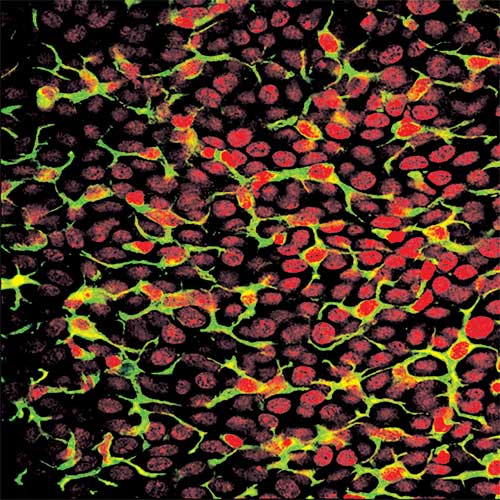
Réseau de cellules inflammatoires à la surface de la conjonctivite © Institut de la Vision.
Rédaction Serge Picaud & Pr José-Alain Sahel - Institut de la Vision
SUITE dans le lien "A lire aussi" ci-dessous : "13 progrès à l'Institut de la Vision, 2e partie"
Photo en vignette : © Institut de la Vision - SU_LArdhuin
Soutenez la recherche, soutenez l'Institut de la Vision >

À lire aussi

Institut de la Vision : l'excellence au féminin
Nos portraits de 7 chercheuses à la pointe de l'innovation
Généticiennes, neurobiologistes, biologistes, physiciennes… : chaque jour, des chercheuses à la pointe de l’innovation font avancer la connaissance des pathologies oculaires, œuvrent au dévelo

13 progrès à l'Institut de la Vision, 2e partie
Le voyage passionnant à travers les avancées majeures de la recherche fondamentale dans le domaine de la vision se poursuit dans cette deuxième partie dédiée à l'extraordinaire travail accompli à l'Institut de la Visio

La dégénérescence maculaire liée à l'âge : DMLA








